
Video: Come si calcola la concentrazione da una curva di titolazione?
2024 Autore: Michael Samuels | [email protected]. Ultima modifica: 2023-12-16 01:46
Dividere il numero di moli di analita presente per il volume originale dell'analita. Ad esempio, se il volume originale dell'analita era di 500 mL, dividere per 1000 mL per L per ottenere 0,5 L. Dividere 0,01 moli di analita per 0,5 L per ottenere 0,02 moli per litro. Questo è il concentrazione o molarità.
Inoltre, come si calcola la concentrazione dalla titolazione?
Utilizzo il formula di titolazione . Se il titolante e l'analita hanno un rapporto molare 1:1, il formula è molarità (M) dell'acido x volume (V) dell'acido = molarità (M) della base x volume (V) della base. (La molarità è la concentrazione di una soluzione espressa come numero di moli di soluto per litro di soluzione.)
Sapete anche, qual è la formula per la concentrazione? Lo standard formula è C = m/V, dove C è il concentrazione , m è la massa del soluto disciolto e V è il volume totale della soluzione.
In secondo luogo, come si trova il punto di equivalenza su una curva di titolazione?
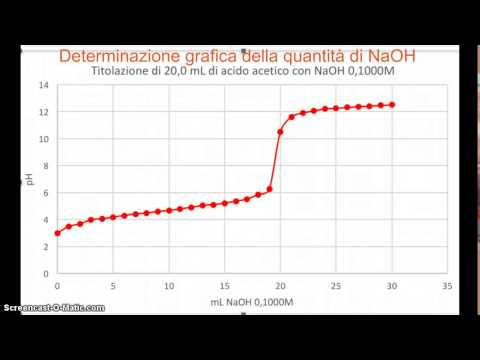
Sul curva , il punto d'equivalenza si trova dove il grafico è più ripido. C'è un rapido e brusco cambiamento di pH intorno a questo punto , che può essere osservato dal cambiamento di colore che avviene durante titolazione . Al punto d'equivalenza , è necessaria una tabella ICE per determinare il volume e l'acidità.
Come si calcola la concentrazione di NaOH?
Calcolo il concentrazione di NaOH dai dati di titolazione è piuttosto semplice la stechiometria: moli NaOH = moli di acido, quindi dividere per volume in L. Un campione di 25,0 ml di 0,105 mol L-1 NaOH e un campione di 50,0 ml di 0,240 mol L-1 NaOH vengono miscelati e la soluzione viene portata a 100,00 ml aggiungendo acqua a sufficienza.
Consigliato:
Cosa ti dice la curva di titolazione?

Una curva di titolazione è un grafico che mostra la variazione del pH della soluzione nella beuta quando il reagente viene aggiunto dalla buretta. Una curva di titolazione può essere utilizzata per determinare: 2) Il pH della soluzione al punto di equivalenza dipende dalla forza dell'acido e dalla forza della base utilizzata nella titolazione
Cosa posso prendere per migliorare la concentrazione e la concentrazione?

10 potenziamenti naturali della concentrazione Metti dei limiti al tempo davanti allo schermo. Tieni traccia delle ore trascorse al computer. Non saltare mai la colazione. Prova gli integratori di ginkgo. Ginseng. Aumenta l'assunzione di vitamina B6. Dormi bene la notte. Bere caffè. Mangia cioccolato fondente
Come si trova il punto finale in una titolazione potenziometrica?

In una titolazione potenziometrica il punto finale è determinato mediante l'uso di una coppia di elettrodi o di un elettrodo combinato. L'endpoint si verifica dove c'è un tasso massimo di variazione del potenziale all'endpoint della titolazione
Come si chiama quando le molecole si spostano da una concentrazione alta a una bassa?

Trasporto attivo attraverso le membrane cellulari. Ci sono numerose situazioni negli organismi viventi in cui le molecole si spostano attraverso le membrane cellulari da un'area a minore concentrazione verso un'area a maggiore concentrazione. Questo movimento dalle aree ad alta concentrazione a quelle basse è chiamato diffusione
Qual è il punto di equivalenza in una curva di titolazione?

(In una titolazione acido-base, c'è una stechiometria acido:base 1:1, quindi il punto di equivalenza è il punto in cui le moli di titolante aggiunte sono uguali alle moli di sostanza inizialmente nella soluzione che viene titolata.) Notare che il pH aumenta prima lentamente, poi rapidamente man mano che si avvicina al punto di equivalenza
